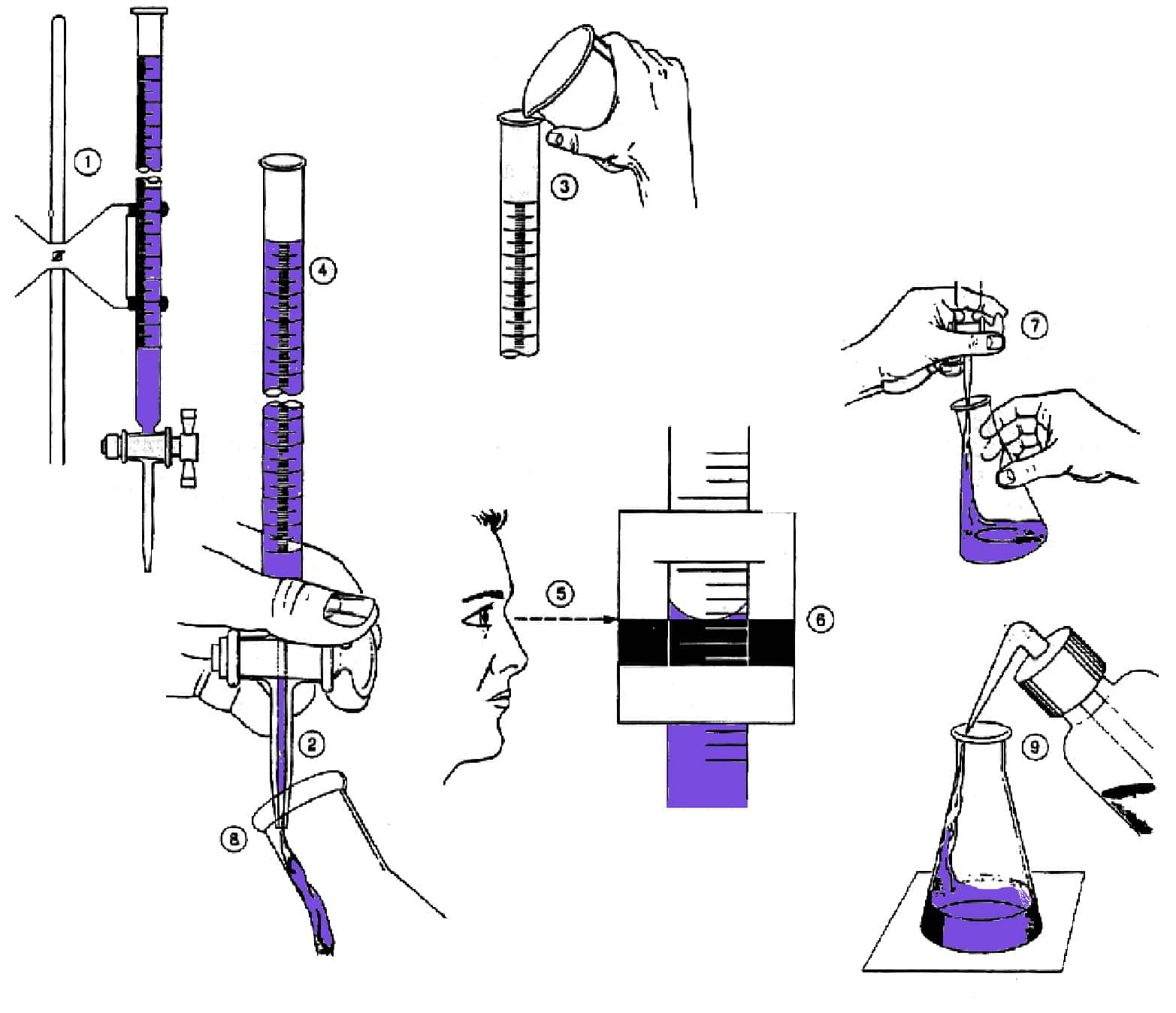
Titrasi asam-basa merupakan suatu cara yang cukup teliti untuk menentukan konsentrasi suatu asam atau basa. Konsentrasi suatu asam ditentukan dengan cara menitrasi asam dengan basa yang telah diketahui kadarnya, begitu puia sebaliknya. Titrasi asam kuat basa kuat dinamakan pula reaksi netralisasi atau penetralan karena pada reaksi menghasilkan garam dan air. Dalam titrasi asam-basa, zat penitrasi disebut sebagai titran atau titer, sedangkan zat yang dititrasi disebut titrat. Titran merupakan larutan baku yang telah diketahui konsentrasinya dan ditempatkan di dalam buret. Titrat merupakan zat yang dianalisis dan belum diketahui konsentrasinya, ditempatkan dalam erlenmeyer yang berada tepat di bawah buret berisi titran.
Sebelum proses titrasi berlangsung, ke dalam titrat ditambahkan indikator asam-basa untuk mengetahui titik akhir titrasi. Indikator asam-basa akan menunjukkan perubahan warna apabiia titik ekuivalen telah tercapai. Titik ekuivalen adalah keadaan yang secara stoikiometri titran dan titrat tepat habis bereaksi. Saat titik ekuivalen tercapai, konsentrasi asam sama dengan konsentrasi basa atau jumlah mol ekuivalen basa yang ditambahkan sama dengan jumlah mol ekuivalen asam yang dinetralkan.
Stoikiometri Larutan Asam-Basa
Indikator asam-basa biasanya bersifat asam lemah. Indikator asam-basa akan memberikan warna yang berbeda dalam asam maupun dalam basa.Ketika titrasi mencapai titik ekuivalen, mol ekuivalen asam sama dengan mol ekuivalen basa. Mol ekuivalen diperoleh dari hasil perkalian antara normalitas (N) dengan volume (V). Rumus ini ditulis sebagai berikut.
Vasam x Nasam = Vbasa x Nbasa
Normalitas (N) diperoleh dari hasil perkalian antara molaritas (M) dengan jumlah mol ion H+ dari asam atau jumlah mol ion OH- dari basa.
Vasam x M x n = Vbasa x M x n
Keterangan:
V = volume
N = normalitas
M = Molaritas
n = jumlah ion H+ (pada asam) atau ion OH (pada basa)
Grafik Titrasi Asam-Basa
Titrasi asam-basa dibedakan menjadi tiga jenis, yaitu titrasi asam kuat-basa kuat, titrasi asam lemah-basa kuat, dan titrasi basa lemah-asam kuat. Titrasi asam-basa dapat digambarkan dengan sebuah grafik titrasi. Grafik titrasi menyatakan perubahan pH pada proses titrasi.
Titrasi Asam Kuat-Basa Kuat

Contoh titrasi asam kuat-basa kuat terjadi pada larutan HN03 0,1 M dengan larutan NaOH 0,1 M. Titrasi antara larutan HN03 0,1 M sebanyak 25 ml dengan larutan NaOH 0,1 M dapat digambarkan
Titik ekuivalen terjadi pada pH 7 saat volume NaOH 25 ml. Pada saat titrasi berlangsung daerah sekitar titik ekuivalen terjadi perubahan pH yang cukup drastis. Titik ekuivalen pada titrasi asam kuat dengan basa kuat dapat ditunjukkan dengan indikator metil merah, bromtimol biru, dan fenolftalein.
Titrasi asam lemah-basa kuat
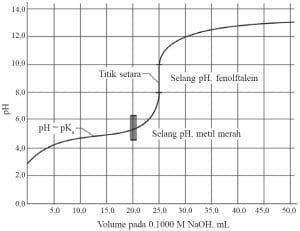
Contoh titrasi asam lemah-basa kuat terjadi pada larutan HCOOH 0,1 M dengan larutan NaOH 0,1 M. Titrasi antara larutan HCOOH 0,1 M sebanyak 25 ml dengan larutan NaOH 0,1 M dapat digambarkan dengan Grafik di samping.
Pada titrasi asam lemah-basa kuat, perubahan pH di sekitar titik ekuivalen terjadi pada pH di atas 7 hingga pH 10. Titik akhir titrasi diharapkan sedekat mungkin dengan titik ekuivalen. Indikator metil merah akan menunjukkan perubahan warna jauh sebelum titik ekuivalen tercapai. Oleh karena itu, indikator yang tepat untuk menunjukkan titik ekuivalen ini adalah fenolftalein.
Titrasi Basa Lemah-Asam Kuat
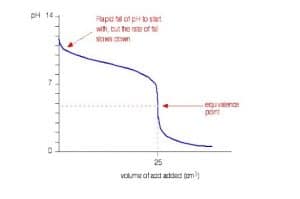
Contoh titrasi basa lemah-asam kuatterjadi pada larutan NH4OH 0,1 M dengan larutan HCI 0,1 M. Titrasi antara larutan NH4OH 0,1 M sebanyak 25 ml dengan larutan HCI 0,1 M dapat digambarkan dengan Grafik berikut.
Pada titrasi ini, perubahan pH di sekitar titik ekuivalen berkisar antara ±7 – ±4. Titik ekuivalen terjadi pada pH di bawah 7 sehingga indikator yang sesuai digunakan adalah metil merah. Indikator fenolftalein tidak digunakan dalam titrasi basa lemah dengan asam kuat karena indikator fenolftalein akan menunjukkan perubahan warna jauh sebelum titik ekuivalen tercapai.
Demikian penjelasan yang bisa kami sampaikan tentang Pengertian Tritrasi,Stoikiometri Larutan Dan Grafik Titrasi Asam-Basa. Semoga postingan ini bermanfaat bagi pembaca dan bisa dijadikan sumber literatur untuk mengerjakan tugas. Sampai jumpa pada postingan selanjutnya.
Baca postingan selanjutnya:
- Peranan dan Pemanfaatan Asam Basa dalam Berbagai Bidang
- Menghitung pH Larutan Asam Lemah dan Basa Lemah
- Penentuan pH Asam Kuat Dan Basa Kuat
- Konsep pH, pOH, dan pKw Pada Larutan Asam Basa
- Mengkaji Dan Mengidentifikasi Sifat Larutan Asam dan Basa
- Teori – Teori dan Konsep Asma Basa Menurut Para Ahli Dan Penjelasan
- Contoh Soal Kimia Dan Pembahasan Terlengkap Tentang Reaksi Kesetimbangan
Originally posted 2024-04-01 18:55:54.